
Naturvidenskabelig pointe:
Man kan undersøge, hvilket grundstof der er tale om ved at se på deres lysudsendelse f.eks. i en forbrænding. Magnesium kan man for eksempel genkende fordi det brænder hvidt.
Intro til lederen
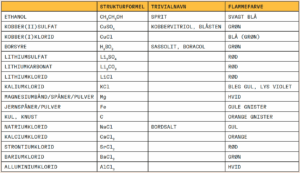
Nogle grundstoffer udsender meget kraftigt lys på de karakteristiske bølgelængder, og det kan man bruge til at farve flammer med i fyrværkeri. Man kan også bruge lysudsendelsen til at måle, hvilke grundstoffer der er i en prøve. Ved analysemetoder som “flamme spektroskopi” og “induktivt koblet plasma spektrometri” , hvor man ud fra farven af en gasflamme måle grundstoffer i meget lave koncentrationer. Det er forskellige elektronovergange i metalionerne der giver farverne. For Lithium, Natrium, Kobber eksiteres elektronerne og når elektronerne vender tilbage til deres oprindelige bane udsendes den karakteristiske lys-farve. Kul, jern og magnesium kan brænde, så der er det forbrændingen i partiklen, der giver energien til lysudsendelsen Man kan generelt bruge mange forskellige salte og et udvalg er nævnt her. F.eks. er der ofte salte i farver og man kan ved at brænde reklamer ofte se den grønne kobberfarve. Tabellen herunder viser at man kan lave mange forskellige farver ved at lave flammefarver. Det er langt fra alle stofferne der bruges i forsøget her – flere af dem er giftige. Brug kun dem, der står beskrevet i “Det skal du bruge”.
Intro til spejderen
Som spejdere laver vi tit bål. Ild og sprit kan sammen med nogle metalforbindelser give flammerne farver. Når stoffer varmes op, udsender de lys. Det er både en udstråling i alle bølgelængder og stråling med karakteristiske bølgelængder, som passer med energi-overgange i stoffet. Kul, jern og magnesium kan brænde, så der er det forbrændingen i partiklen, der giver energien til lysudsendelsen.
Indledende spørgsmål
1. Hvorfor udsender metallerne forskellige farver?
2. Hvor kan man finde metallerne i hverdagen?
3. Hvor kan man få kulstøv?
4. Hvordan kunne man lave jernspåner?
Aktivitetsbeskrivelse
Sådan gør du:
Opskriften er for 1 patrulje/gruppe
OBS. Alle i patruljen skal bære
beskyttelsesbriller.
- Lav en 2 meter lang rende i alufolie
- Folien foldes i 4 lag og det krølles sammen i siderne og enderne så det danner en 8-10 cm bred rende, der er tæt
- Folierenden placeres på brættet
- Folierenden fyldes med 1 kg salt
- 1 L sprit hældes over salten
- Spritten tændes
- Drys salte over renden – de skal spredes godt og drysses fra 30-50 cm over renden, så man kan nå at se flammefarven. Hver gang I bruger en ny salt, så drys dem et ubrugt sted på renden
- 10 g Kobbersulfat (CuSO4) også kaldet kobbervitriol eller blåsten – grøn flamme
- 1 spsk Knust kul (C) – orange gnister
- 1 spsk Jernpulver eller spåner (Fe) – gule gnister.
- Sæt 5 cm magnesiumbånd fast med på en pind og hold det ind i flammerne så det antændes (lad være at kigge direkte på det kraftige hvide lys)
- Drys ½ dL flødepulver over renden – det skal spredes godt og drysses fra 30-50 cm over renden, så man får en stor overflade.
- Drys en håndfuld af den tørrede mel på flammerne.
Afrunding
Overvej dette efter aktiviteten:
1. Hvorfor er farverne forskellige?
2. Hvorfor blusser flammerne op når man drysser flødepulver over renden
Børn og unge bestemmer:
Prøv at kombinere med brændende klæde,
hvor der går ild i klædet mens man drysser
salte over renden. Lad spejderne være kreative
omkring, hvad der vil kunne drysses
Der er brandfare ved brug af åben ild. Hold aldrig hovedet ind over varmekilden og hav altid vinden i ryggen. Brug beskyttelsesbriller. Saltbøsserne skal mærkes tydeligt med indhold og faremærkater. Når de først har været brugt til eksperimenter, må de ikke bruges til fødevarer igen. Affald kan, efter afkøling, smides i skraldespanden for de kemikalier, der er med i forsøget.
Saltbøsserne gemmes til næste gang.




